PROPIEDADES PERIÓDICAS
Son propiedades que presentan los elementos químicos y que se repiten secuencialmente en la tabla periódica. Por la colocación en la misma de un elemento, podemos deducir que valores presentan dichas propiedades así como su comportamiento químico.
Radio atómico
El radio atómico representa la distancia que existe entre el núcleo y la capa de valencia (la más externa). Por medio del radio atómico es posible determinar el tamaño del átomo. Dependiendo del tipo de elemento, existen diferentes técnicas para su determinación como la difracción de neutrones, de electrones o de rayos X. En cualquier caso no es una propiedad fácil de medir ya que depende, entre otras cosas, de la especie química en la que se encuentre el elemento en cuestión.
En un grupo cualquiera el radio atómico aumenta desde arriba hacia abajo debido al aumento en el nº de niveles de E.
En los períodos, el radio atomico disminuye al aumentar el número atómico (Z), hacia la derecha, debido a la atracción que ejerce el núcleo sobre los electrones de los orbitales más externos, disminuyendo así la distancia núcleo-electrón.
El radio atómico puede ser o covalente o metálico. La distancia entre núcleos de átomos "vecinos" en una moléculas es la suma de sus radios covalentes, mientras que el radio metálico es la mitad de la distancia entre núcleos de átomos "vecinos" en cristales metálicos. Usualmente, cuando se habla de radio atómico, se refiere a radio covalente.
Energía de ionización
La
energía de ionización,
potencial de ionización o
EI es la energía necesaria para arrancar un electrón de un átomo perteneciente a una sustancia que se encuentra en estado gaseoso.
La reacción puede expresarse de la siguiente forma:
Siendo
A(g) los átomos neutros de una sustancia elemental en estado gaseoso;
EI, la energía de ionización y
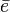
un electrón.
Esta energía corresponde a la primera ionización. El segundo potencial de ionización representa la energía precisa para sustraer el segundo electrón; este segundo potencial de ionización es siempre mayor que el primero, pues el volumen de un ion positivo es menor que el del átomo y la fuerza electrostática es mayor en el ion positivo que en el átomo, ya que se conserva la misma carga nuclear.
El potencial o energía de ionización se expresa en electrón-voltio, Julios o en kilo Julios por mol (kJ/mol).
1 eV = 1,6 × 10-19 C × 1 V = 1,6 × 10-19 J
En los elementos de una misma familia o grupo el potencial de ionización disminuye a medida que aumenta el número atómico, es decir, de arriba abajo.
Sin embargo, el aumento no es continuo, pues en el caso del berilio y el nitrógeno se obtienen valores más altos que lo que podía esperarse por comparación con los otros elementos del mismo período. Este aumento se debe a la estabilidad que presentan las configuraciones s2 y s2 p3,respectivamente.
La energía de ionización más elevada corresponde a los gases nobles, ya que su configuración electrónica es la más estable, y por tanto habrá que proporcionar más energía para arrancar los electrones.
Potencial de Ionización
El Potencial de ionización (P&) es la energía mínima requerida para separar un electrón de un átomo o molécula especifica a una distancia tal que no exista interacción electrostática entre el ion y el electrón. Inicialmente se definía como el potencial mínimo necesario para que un electrón saliese de un átomo que queda ionizado. El potencial de ionización se medía en voltios. En la actualidad, sin embargo, se mide en electrón-voltios (aunque no es una unidad del SI) o en julios por mol. El sinónimo energía de ionización (El) se utiliza con frecuencia. La energía para separar el electrón unido más débilmente al átomo es el primer potencial de ionización; sin embargo, hay alguna ambigüedad en la terminología. Así, en química, el segundo potencial de ionización del litio es la energía del proceso.
Tabla periódica del primer potencial de ionización, en kJ/mol Afinidad electrónica
La
afinidad electrónica (AE) o
electroafinidad se define como la energía involucrada cuando un átomo gaseoso neutro en su estado fundamental (de mínima energía) captura un electrón y forma un ion mononegativo:

. Dado que se trata de energía liberada, tiene signo negativo. En los casos en los que la energía sea absorbida, tendrá signo positivo.
La electroafinidad aumenta cuando el tamaño del átomo disminuye, el efecto pantalla aumenta y cuando el nº atómico disminuye. Visto de otra manera: aumenta de izquierda a derecha, y de abajo hacia arriba, al igual que lo hace la electronegatividad. En la tabla periódica tradicional no es posible encontrar esta información.
- O bien el cambio de energía que ocurre cuando un átomo en estado gaseoso acepta un electrón para formar un ion.
Tabla periódica de afinidades electrónicas, en kJ/mol
Electronegatividad
La electronegatividad, denotada por el símbolo χ (letra griega chi) es una propiedad química que mide la capacidad de un átomo (o de manera menos frecuente un grupo funcional) para atraer hacia él los electrones, o densidad electrónica, cuando forma un enlace covalente en una molécula.
La electronegatividad de un átomo determinado está afectada fundamentalmente por dos magnitudes, su masa atómica y la distancia promedio de los electrones de valencia con respecto al núcleo atómico. Esta propiedad se ha podido correlacionar con otras propiedades atómicas y moleculares. Fue Linus Pauling el investigador que propuso esta magnitud por primera vez en el año 1932, como un desarrollo más de su teoría del enlace de valencia.
La electronegatividad no se puede medir experimentalmente de manera directa como, por ejemplo, la energía de ionización, pero se puede determinar de manera indirecta efectuando cálculos a partir de otras propiedades atómicas o moleculares.
Se han propuesto distintos métodos para su determinación y aunque hay pequeñas diferencias entre los resultados obtenidos todos los métodos muestran la misma tendencia periódica entre los elementos.
El procedimiento de cálculo más común es el inicialmente propuesto por Pauling. El resultado obtenido mediante este procedimiento es un número adimensional que se incluye dentro de la escala de Pauling. Escala que varía entre 0,7 para el elemento menos electronegativo y 4,0 para el mayor.
Electronegatividades de los elementos
|
| Grupo (Vertical) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| Período (Horizontal) |
|
| 1 | H
2.20 |
| He
|
| 2 | Li
0.98 | Be
1.57 |
| B
2.04 | C
2.55 | N
3.04 | O
3.44 | F
3.98 | Ne
|
| 3 | Na
0.93 | Mg
1.31 |
| Al
1.61 | Si
1.90 | P
2.19 | S
2.58 | Cl
3.16 | Ar
|
| 4 | K
0.82 | Ca
1.0 | Sc
1.36 | Ti
1.54 | V
1.63 | Cr
1.66 | Mn
1.55 | Fe
1.83 | Co
1.88 | Ni
1.91 | Cu
1.90 | Zn
1.65 | Ga
1.81 | Ge
2.01 | As
2.18 | Se
2.55 | Br
2.96 | Kr
3.00 |
| 5 | Rb
0.82 | Sr
0.95 | Y
1.22 | Zr
1.33 | Nb
1.6 | Mo
2.16 | Tc
1.9 | Ru
2.2 | Rh
2.28 | Pd
2.20 | Ag
1.93 | Cd
1.69 | In
1.78 | Sn
1.8 | Sb
2.05 | Te
2.1 | I
2.66 | Xe
2.60 |
| 6 | Cs
0.79 | Ba
0.89 | *
| Hf
1.3 | Ta
1.5 | W
2.36 | Re
1.9 | Os
2.2 | Ir
2.2 | Pt
2.28 | Au
2.54 | Hg
2.00 | Tl
1.62 | Pb
2.33 | Bi
2.02 | Po
2.0 | At
2.2 | Rn
2.2 |
| 7 | Fr
0.7 | Ra
0.9 | **
| Rf
| Db
| Sg
| Bh
| Hs
| Mt
| Ds
| Rg
| Cn
| Uut
| Uuq
| Uup
| Uuh
| Uus
| Uuo
|
|
| Lantánidos | *
| La
1.1 | Ce
1.12 | Pr
1.13 | Nd
1.14 | Pm
1.13 | Sm
1.17 | Eu
1.2 | Gd
1.2 | Tb
1.1 | Dy
1.22 | Ho
1.23 | Er
1.24 | Tm
1.25 | Yb
1.1 | Lu
1.27 |
| Actínidos | **
| Ac
1.1 | Th
1.3 | Pa
1.5 | U
1.38 | Np
1.36 | Pu
1.28 | Am
1.13 | Cm
1.28 | Bk
1.3 | Cf
1.3 | Es
1.3 | Fm
1.3 | Md
1.3 | No
1.3 | Lr
1.3 |




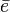 un electrón.
un electrón. . Dado que se trata de energía liberada, tiene signo negativo. En los casos en los que la energía sea absorbida, tendrá signo positivo.
. Dado que se trata de energía liberada, tiene signo negativo. En los casos en los que la energía sea absorbida, tendrá signo positivo.